রাসায়নিক বন্ধন কাকে বলে ? আয়নিক বন্ধন কাকে বলে ? উদাহরণ সহ ব্যাখ্যা কর ?
রাসায়নিক
বন্ধন : কোনো অনুতে উপাদান পরমাণু গুলো পরস্পর যে আর্কষণ
শক্তির মাধ্যমে যুক্ত থাকে তাকে রাসায়নিক বন্ধন বলা হয়।
আয়নিক
বন্ধন : ধাতব পরমাণু ও অধাতব পরমাণু ইলেকট্রন বর্জন ও
গ্রহনের মাধ্যমে যে বন্ধন তৈরি করে তাকে আয়নিক বন্ধন বলা হয়।
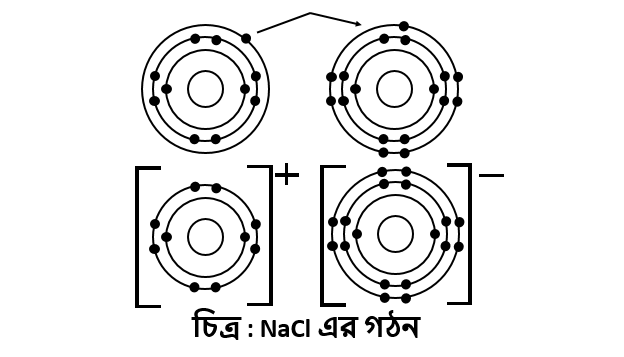
নিচে NaCl এর বন্ধন গঠন কৌশল
চিহ্ন সহ বিশ্লেষণ করা হলো :
Na ও Cl এর ইলেকট্রন বিন্যাস নিম্নরূপ :
Na(11) ➡ 1s22s22p63s1
Cl(17) ➡ 1s22s22p63s23p5
ইলেকট্রন বিন্যাস থেকে দেখা
যাচ্ছে যে, Na ও Cl এর শেষ কক্ষপথে ইলেকট্রন সংখ্যা যথাক্রমে 1 ও 7 টি।
স্থিতিশীলতা অর্জনের জন্য Na
পরমাণু তার সর্বশেষ কক্ষপথের 1টি ইলেকট্রন বর্জন করে Na+ আয়ন
গঠন করে এবং Cl পরমাণু তার সর্বশেষ কক্ষপথে 1 টি ইলেকট্রন গ্রহণ করে Cl- আয়ন গঠন করে।
আরো জানুন,
১. NH3, CH4 এবং CCl4 সমযোজী অনুর গঠন।
২. রাসায়নিক বন্ধন কাকে বলে ? উদাহরণ সহ ব্যাখ্যা কর ?
৩. সরণ কাকে বলে ? এর একক ও মাত্রা নির্ণয় কর ?
এদের আয়নিক সমীকরণ নিম্নরূপ :
Na-e⟶Na+-------------x2
Cl2+e⟶2Cl-
一一一一一一一一一一一一一一一一
2Na + Cl2 ⟶2Na+ + 2Cl-
বা, 2Na + Cl2 ⟶2NaCl
এই বিপরীদ ধর্মী আয়ন দুটি পরস্পর
স্থির বৈদ্যুতিক আকর্ষণ বল দ্বারা যুক্ত হয়ে NaCl নামক আয়নিক যৌগ উৎপন্ন করে।
ডায়াগ্রাম
:

Post a Comment